
Эффект плацебо и антидепрессанты!
Natallia Niachai Просмотров: 3327
Считается, что антидепрессанты работают путем устранения химического дисбаланса, особенно недостатка серотонина в мозге (это важно знать, чтобы понять эффект плацебо и антидепрессанты). Но анализ опубликованных и неопубликованных данных, которые были скрыты производителями лекарств, показал, что большинство (если не все) выгоды связаны с эффектом плацебо. Некоторые антидепрессанты повышают уровень серотонина, другие снижают их, а другие вообще не влияют на серотонин.
Тем не менее, все они показывают одинаковые терапевтические преимущества. Вместо того, чтобы лечить депрессию, некоторые распространенные антидепрессанты могут вызывать биологическую уязвимость, что делает людей более склонными к депрессии впоследствии. Другие виды лечения (например, психотерапия и физическая подготовка) дают те же краткосрочные преимущества, что и антидепрессанты, но показывают лучшую долгосрочную эффективность и без побочных эффектов и риска для здоровья от приема лекарств.
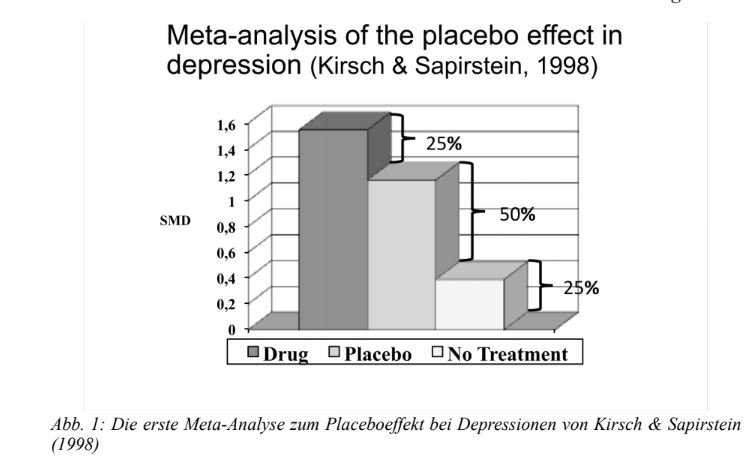
Когда мы с Сапирштейном начали анализировать данные клинических испытаний антидепрессантов, нас особенно не интересовали антидепрессанты. Скорее, мы были заинтересованы в понимании эффекта плацебо, как и во всей моей академической карьере. Я спросил себя: как получается, что вера в то, что вы приняли лекарство, может вызвать некоторые эффекты этого лекарства?
Мы с Сапирштейном чувствовали, что депрессия полезна для наблюдения за эффектами плацебо. В конце концов, одной из основных характеристик депрессии является чувство безнадежности, которое испытывают подавленные люди. Если вы спросите у людей, страдающих депрессией, что хуже в их жизни, многие ответят, что это их депрессия. Британский психолог Джон Теасдейл назвал это «депрессией по поводу депрессии». Если это так, то обещание эффективного лечения само по себе может облегчить депрессию, поскольку надежда заменяет безнадежность, надежду на то, что вы в конечном итоге выздоровеете. Имея это в виду, мы решили измерить эффект плацебо при депрессии.
Сапирштейн и я исследовали литературные исследования, в которых пациентам случайным образом давали либо неэффективное плацебо, либо вообще никакого лечения. Исследования, которые мы обнаружили, также содержали данные об ответной реакции на антидепрессанты, потому что только здесь приведены данные об ответной реакции на плацебо у пациентов с депрессией. Меня не особо интересовали эффекты лекарства. Я предположил, что антидепрессанты были эффективны.
Как психотерапевт, я иногда направлял своих пациентов с серьезной депрессией к врачам, чтобы им могли назначать антидепрессанты. Иногда состояние моих пациентов улучшалось, когда они начали принимать антидепрессанты, иногда нет. Если они почувствовали себя лучше, я предполагал, что это из-за эффекта препарата. Учитывая мой давний интерес к эффекту плацебо, я должен был бы догадаться, что скорее всего это «эффект плацебо», но в то время это было не так актуально.
Когда мы с Сапирштейном проанализировали полученные данные, мы не были удивлены, обнаружив решающий эффект плацебо при депрессии. Однако, что нас удивило: как мало эффект от лекарств. 75% улучшение в группе лечения также произошло, когда пациенты получали пустышку без каких-либо активных веществ. Излишне говорить, что наш метаанализ оказался очень спорным. Их публикация привела к горячим спорам. Реакция критиков заключалась в том, что эти данные не могли быть правильными. Возможно наше исследование могло бы привести нас к анализу нерепрезентативного набора клинических испытаний. Критики сказали, что антидепрессанты были оценены во многих тестах, и их эффективность была хорошо документирована.
Чтобы ответить на критику, мы решили повторить наше исследование, используя другой набор клинических тестов (Kirsch et al., 2002). Для этого мы использовали Закон о свободе информации (FOIA) 1), чтобы запросить у Управления по контролю за продуктами и лекарствами (FDA) 2) документы, которые фармацевтические компании представили в ходе процесса одобрения для признания шести новых поколений антидепрессантов. На которые были выписаны большинство рецептов в то время. Этот сбор данных FDA имеет ряд преимуществ. Самое главное, что FDA требует от фармацевтических компаний предоставлять информацию обо всех клинических исследованиях, которые они спонсируют. Например, у нас были данные как неопубликованных, так и опубликованных исследований. Это оказалось очень важным. Почти половина всех клинических испытаний, спонсируемых фармацевтическими компаниями, не были опубликованы. Только фармацевтические компании и FDA знали результаты неопубликованных тестов, и почти все они не смогли найти значительного преимущества препарата по сравнению с плацебо. Второе преимущество наборов данных FDA заключается в том, что для всех собранных данных использовался один и тот же прибор для измерения депрессии - гамильтонова шкала депрессии (HAM-D). Это облегчило понимание клинической важности различия между приемом лекарств и плацебо. В конце концов, данные в сборе данных FDA формируют основу для одобрения лекарства, поэтому у него особый статус. Если бы что-то не так с этими тестами, лекарства не были бы одобрены вообще. По данным, которые мы получили от FDA, только 43% протестированных лекарств были статистически значимыми по сравнению с плацебо. Остальные 57% были неудачными или отрицательными.
Наш анализ показал, что действие антидепрессантов и плацебо на эти антидепрессанты составило 82% на основе эффектов плацебо. В результате мы с коллегами повторили наш мета-анализ по большему количеству тестов, представленных в FDA (Kirsch et al., 2008). С этим расширенным количеством данных мы снова обнаружили, что 82% эффекта от лекарственного препарата был удвоен из-за эффекта плацебо. Что еще более важно, в обоих анализах средняя разница между препаратом и плацебо была менее двух баллов по шкале HAM-D. Это состоит из 17 пунктов, и испытуемые могут набрать от 0 до 53 баллов, в зависимости от степени их депрессии. 6 баллов могут быть связаны с изменением режима сна, без изменения других симптомов депрессии. Таким образом, разница в 1,8 балла, которую мы обнаружили между лекарством и плацебо, была на самом деле очень мала - достаточно мала, чтобы не иметь клинически значимого значения (см. Рис.2). Но вы не должны верить только мне, насколько мала эта разница. Национальный институт здравоохранения и клинического мастерства (NICE), который разрабатывает руководящие принципы лечения для Национальной службы здравоохранения в Соединенном Королевстве, определил разницу в 3 балла между приемом лекарств и плацебо на HAM-D в качестве критерия клинической значимости (NICE), 2004). Если объединить опубликованные и неопубликованные данные, то нет существенной разницы между антидепрессантами и неэффективными плацебо.
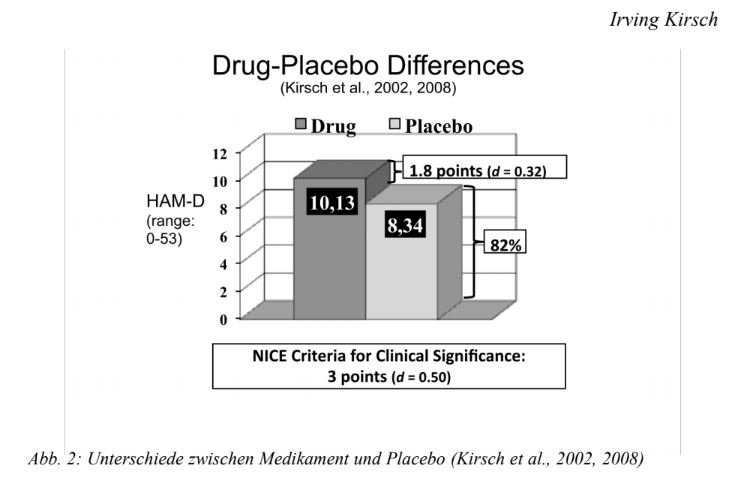
Утверждалось, что критерий NICE был произвольным (например, Turner & Rosental, 2008), и это правда. Это так же произвольно, как p <0,5, чтобы быть выбранным в качестве критерия статистической значимости. Тем временем, Джоанна Монкрифф и я обнаружили непроизвольный критерий клинической значимости (Moncrieff & Kirsch, 2015). В 2013 году Стефан Лейхт и его коллеги (Leucht et al., 2013) сравнили классификации по шкале HAM-D с классификациями по шкале улучшения общего клинического впечатления (CGI-I) (Guy, 1976). 7-балльная шкала, по которой клиницисты оценивают пациентов от 1 (очень значительное улучшение) до 4 (без изменений) до 7 (намного хуже). Leucht использовал данные пациентов из 43 клинических исследований на 7 131 пациенте и обнаружил, что среднее значение изменения по шкале HAM-D для пациентов, которые были классифицированы как неизмененные по шкале CGI-I, было 3 балла, точно такой критерий, который NICE определил как клинически значимое улучшение (см. рис. 3). Таким образом, проблема с критерием NICE заключается в том, что он слишком неточный. Разница в 3 балла по шкале HAM-D не может быть определена клиницистами среди их пациентов вообще. Более разумным критерием будет изменение в шкале HAM-D, которое соответствует классификации CGI-I как «незначительное улучшение». Согласно данным Leucht et al., Классификация «незначительное улучшение» соответствует снижению на 7 контрольных точек HAM-D.
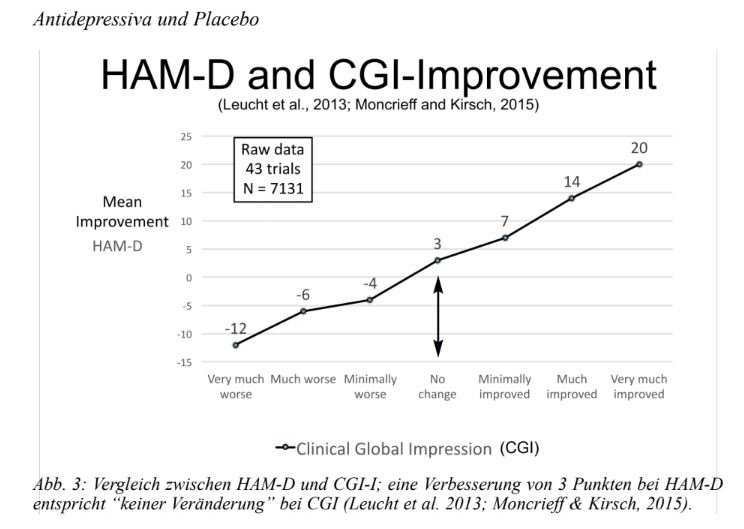
На этом этапе я должен указать на разницу между статистической и клинической значимостью. Статистическая значимость относится к достоверности эффекта. Это фактический эффект или просто случайный? Статистическая значимость ничего не говорит о величине эффекта. Клиническое значение, с другой стороны, связано со степенью эффекта и имеет ли это значение в жизни человека. Например, представьте, что исследование 500 000 человек показало, что улыбка увеличивает продолжительность жизни на пять минут. С 500 000 испытуемых я могу в значительной степени гарантировать, что эта разница будет статистически значимой; клинически, однако, это бессмысленно.
С тех пор наши анализы неоднократно повторялись (Fountoulakis & Möller, 2011; Fournier et al., 2010; NICE, 2004; Turner et al., 2008). Наши данные были использованы для некоторых повторений, другие проанализировали другие клинические испытания. FDA даже провела собственный метаанализ всех одобренных антидепрессантов (Khin et al., 2011). Несмотря на все различия в типе обработки данных, значения остались на удивление стабильными. Различия по шкале HAM-D оставались небольшими повсюду - всегда ниже значения, которое соответствует оценке CGI-I «без изменений» (см. Рис. 4). Томас П. Лафрен, директор Департамента психиатрических продуктов FDA, признал это в программе новостей американского телевидения 60 минут: «Я думаю, что мы все согласны с тем, что изменения, которые видны в краткосрочных тестах, а именно разница в улучшении между приемом лекарств и плацебо довольно мала».
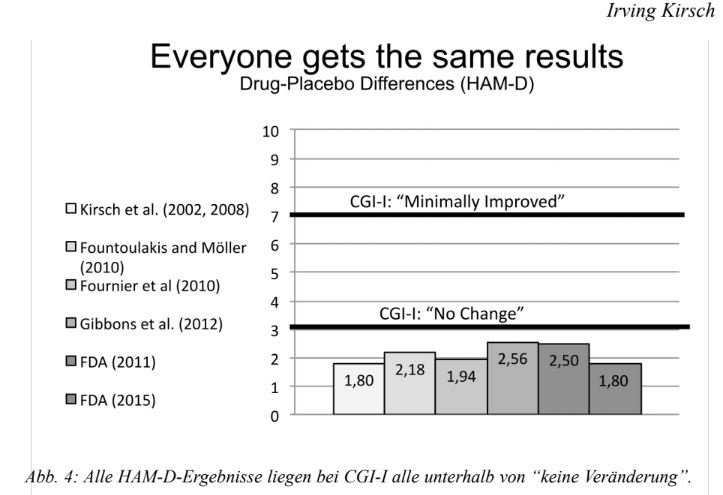
Не только краткосрочные тесты показывают небольшую, клинически незначимую разницу между препаратом и плацебо. В своем метаанализе опубликованных клинических тестов NICE (2004) обнаружила, что даже при длительных обследованиях разница между лекарством и плацебо не была больше, чем при краткосрочных исследованиях. Разница между лекарством и плацебо невелика, настолько мала, что практикующие вообще не могут его обнаружить.
Тяжесть депрессии и эффективность антидепрессантов
В критике нашего мета-анализа 2002 года утверждалось, что наши результаты связаны с клиническими испытаниями на субъектах с меньшей депрессией. Более существенная разница, безусловно, будет обнаружена у пациентов с тяжелой депрессией. Эта критика фактически заставила моих коллег и меня снова проанализировать данные FDA 2008 (Kirsch et al., 2008). Мы классифицировали клинические испытания базы данных FDA, первоначально основанные на тяжести депрессии пациента, используя традиционные категории для депрессии. Было обнаружено, что только одно исследование было проведено на пациентах с умеренной депрессией и что не было существенной разницы между лекарством и плацебо; на самом деле разница была практически нулевой (0,07 балла по шкале HAM-D). Все остальные исследования проводились на пациентах со средним базовым уровнем депрессии «очень тяжелый», и даже у этих пациентов разница между лекарственным средством и плацебо была ниже уровня клинической значимости
Тем не менее, вес имел значение. Пациенты с чрезвычайно тяжелой депрессией, чье значение теста по шкале HAM-D составляло не менее 28, показали среднюю разницу между лекарством и плацебо в 4,36 балла. Это выше критерия клинической значимости, предложенного NICE (2004), но значительно ниже разницы в 7 баллов, что соответствует классификации CGI-I для «минимального улучшения».
Чтобы выяснить, сколько пациентов было в группе с тяжелой депрессией, я попросил Марка Циммермана из Медицинской школы Университета Брауна предоставить мне необработанные данные из исследования, в котором он и его коллеги оценивали результаты теста HAM-D пациентов, который был диагностирован с униполярным большим депрессивным расстройством (MDD) после того, как предстал перед амбулаторной психиатрической практикой (Zimmermann et al., 2005). Только около 10% из этих пациентов имели баллы теста HAM-D 28 или более баллов. Это говорит о том, что 90% пациентов с депрессией не имеют клинически значимого эффекта от назначаемых им антидепрессантов (эффект плацебо и антидепрессанты).
Тем не менее, это значение в 10% может переоценить количество людей, которые получают пользу от антидепрессантов. Антидепрессанты также назначают людям, у которых нет тяжелой депрессии. Любимая собака моего соседа умерла - и доктор прописал ему антидепрессант.
Я не считал, сколько людей сказали мне, что им прописали антидепрессант от бессонницы - хотя бессонница - это частый побочный эффект антидепрессантов. Около 20% страдающих бессонницей в США назначают антидепрессанты своим семейным врачом в качестве лекарства (Simon & VonKorff, 1997), хотя «эта популярность антидепрессантов при бессоннице отнюдь не подтверждается различными убедительными данными, но только мнением и убеждения врачей, прописывающих их»(Wiegand, 2008).
Попытки других исследователей оценить связь между исходной тяжестью и различием между приемом лекарств и плацебо дали разные результаты. Некоторые приходят к тому же соотношению, что и мы (например, Fournier et al., 2010; Khin et al., 2011), в то время как другие не находят связи между серьезностью заболевания и различием между приемом лекарств, и плацебо (например, Fountoulakis et al., 2013; Locher et al., 2015). Но во всех мета-анализах обнаружены общие различия между лекарственным средством и плацебо, которые ниже критериев NICE по клинической значимости. Таким образом, вопрос заключается в следующем: существует ли подгруппа пациентов с тяжелой депрессией, для которых антидепрессанты являются клинически эффективными или им не хватает эффективности на всех стадиях тяжести заболевания?
Прогнозирование ответа на лечение
Одним из немногих прогностических факторов для ответа на лечение депрессии является ее серьезность. Тип антидепрессанта практически не влияет на успех лечения. Следующее резюме мета-анализов 2011 года сравнивает антидепрессанты:
"Основываясь на 234 исследованиях, не было обнаружено никаких существенных различий в эффективности и действенности при лечении острых, продолжающихся и хронических БДР. Не было обнаружено различий в эффективности у пациентов с побочными эффектами или в группах, разделенных по возрасту, полу, этнической принадлежности или сопутствующей патологии [...] Текущие результаты не оправдывают рекомендацию по определенному антидепрессанту второго поколения Основа для различий в эффективности" (Gartlehner et al., 2011)
Хотя природа препарата не вносит клинически значимых изменений в исход, он влияет на реакцию на плацебо. Почти все тесты на антидепрессанты содержат кардиостимулятор на начальной стадии. Перед началом тестирования все пациенты получают плацебо в течение недели или двух. После этой начальной фазы пациенты снова обследуются, и любой, кто значительно улучшился, исключается из дальнейшего тестирования. Это оставляет тех пациентов, которые вообще не получали никакой пользы от плацебо, и тех, кто получал лишь небольшую пользу. Эти пациенты теперь выбираются случайным образом.
В группе разделена на тех, кто получает препарат и тех, кто получает плацебо. Как выясняется, те пациенты, у которых наблюдается хотя бы небольшое улучшение на начальном этапе, чаще всего реагируют на фактический препарат. Это подтверждается не классификацией врачей, а и изменениями функций мозга (Hunter et al., 2006; Quitkin et al., 1998).
Как эти препараты получили одобрение?
Как случилось, что лекарства с такой низкой эффективностью были одобрены FDA? Для этого вам необходимо понять критерии, которые FDA использует для одобрения. FDA требует двух адекватно выполненных клинических испытаний, которые показывают значительную разницу между препаратом и плацебо. Но есть лазейка: нет ограничений на количество тестов, выполненных в поисках двух значимых тестов. Тесты с отрицательным результатом просто не учитываются! Кроме того, клиническое значение результата не принимается во внимание. Единственное, что имеет значение, это статистическая значимость результатов.
Самый возмутительный пример реализации этих критериев можно увидеть в утверждении Viibryd 2011 FDA. Было проведено семь контролируемых тестов эффективности. Первые пять пропустили какую-либо значимую разницу, измеренную любым показателем депрессии, и средняя разница между препаратом и плацебо в этих исследованиях составляла менее половины балла по шкале HAM-D; в двух из этих пяти испытаний разница была в пользу плацебо. Компания провела еще два теста и смогла получить небольшие, но существенные различия между препаратами и плацебо (1,70 балла). Средняя разница по всем семи тестам составила 1,01 балла по шкале HAM-D. Этого было достаточно, чтобы FDA предоставило одобрение и предоставило следующую информацию врачам и пациентам: «Эффективность VIIBRYD определялась в двух 8-недельных, рандомизированных, двойных слепых и плацебо-контролируемых тестах». Тесты, которые предшествовали двум успешным, никогда не упоминались.
Неспособность упомянуть неудачные испытания не была просто недосмотром; это показывает тщательно продуманный принцип, который существовал в течение многих десятилетий. Насколько я знаю, есть только один антидепрессант, который FDA также сообщил о существовании отрицательных тестов. Это – циталопрам. Эта информация была получена из-за возражения, высказанного Полом Лебером, который был тогда директором отдела FDA по нейрофармакологическим препаратам. Во внутренней записке от 4 мая 1998 года Лебер писал:
«Один аспект маркировки заслуживает особого упоминания. [Отчет] не только описывает клинические тесты, которые предоставляют доказательства антидепрессивного действия циталопрама, но также упоминает адекватные и хорошо контролируемые тесты, которые не прошли здесь [...] Директор департамента склонен полагать, что такая информация не имеют никакой практической пользы ни для пациента, ни для выписывающего лекарства врача. Я не согласен. Я полагаю, что и врачу, и пациенту, и третьей стороне в группе, которая платит, не имея прямого доступа к официальным отчетам FDA, полезно узнать, что антидепрессантный эффект циталопрама не был фактически доказан в каждом контролируемом клиническом испытании, который должен был его показать. Мне известно, что клинические испытания часто не подтверждают эффективность эффективных лекарств. Однако я сомневаюсь, что общественность и даже большинство медицинского сообщества знают об этом факте. Я убежден, что они не только имеют право знать, но они должны знать. Кроме того, я считаю, что эта выборочная маркировка, описывая только положительные тесты и исключая отрицательные, может рассматриваться как потенциально «неправильная и вводящая в заблуждение».
Слава Полу Леберту!
Слава Полу Леберу! Я никогда не встречал этого человека чести и не переписывался с ним, но из-за этой записки он один из моих героев.
Перевод статьи Ирвина Кирша
Если есть вопросы или вы хотите обсудить эту тему, напишите мне.




